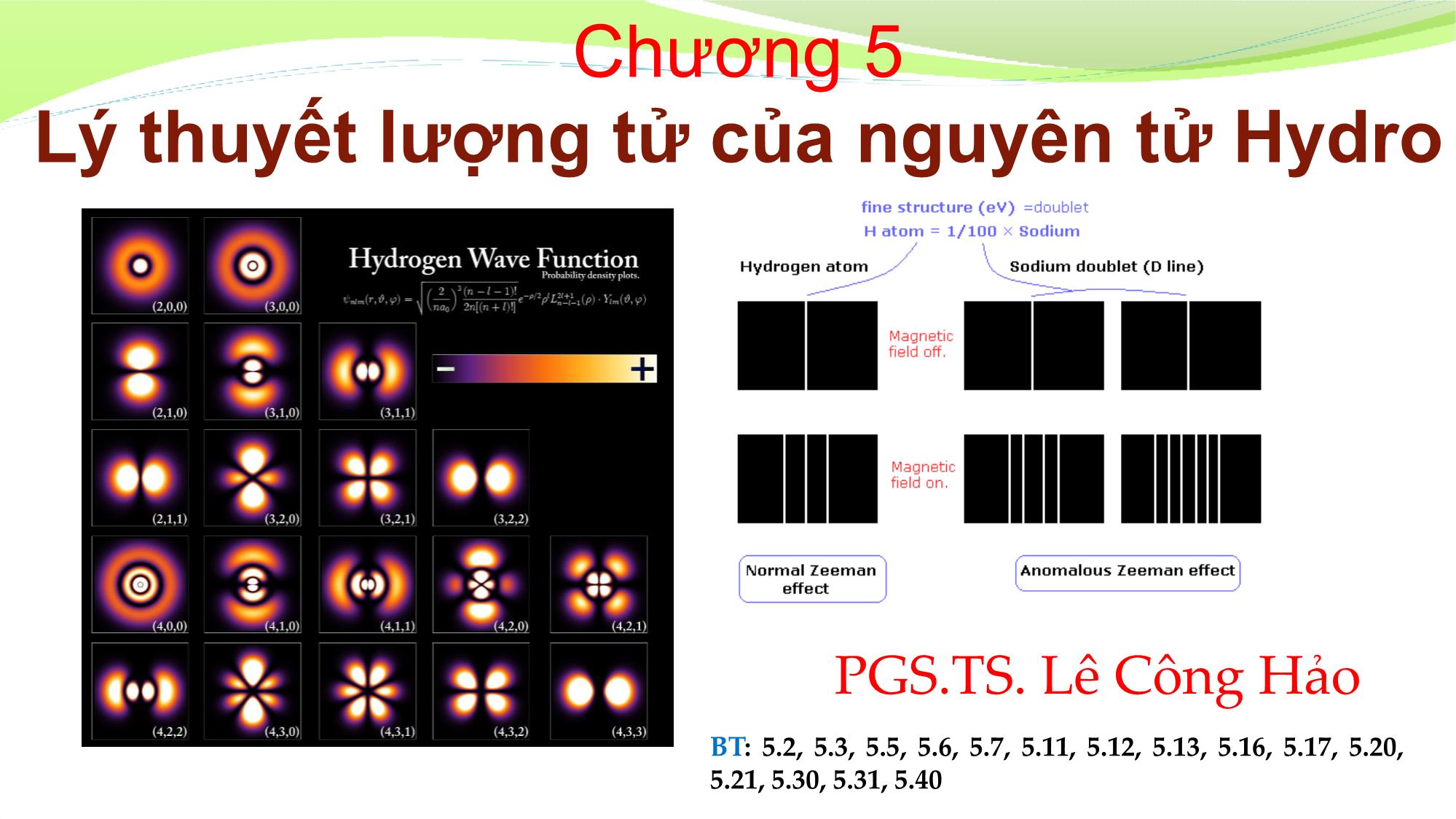
Bài giảng Vật lý đại cương - Chương 5: Lý thuyết lượng tử của nguyên tử Hydro - Lê Công Hảo
Các electron bao giờ cũng có khuynh hướng chiếm mức năng lượng thấp nhất (n nhỏ nhất).
Electron lấp đầy các lớp từ thấp đến cao
Thứ tự lớp:
1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d,
Bảng hệ thống tuần hoàn Mendeleev
Mỗi lớp lại chia thành các lớp con ứng với các trị số khác nhau của ℓ, mỗi lớp con chứa tối đa 2(2ℓ +1) electron.
Ví dụ: Lớp L (n = 2) có 2 lớp con:
- Lớp con S (ℓ = 0) có tối đa 2(2ℓ + 1) = 2 electron,
- Lớp con P (ℓ = 1) có tối đa 6 electron.
Bài giảng Vật lý đại cương - Chương 5: Lý thuyết lượng tử của nguyên tử Hydro - Lê Công Hảo trang 1
Bài giảng Vật lý đại cương - Chương 5: Lý thuyết lượng tử của nguyên tử Hydro - Lê Công Hảo trang 2

Bài giảng Vật lý đại cương - Chương 5: Lý thuyết lượng tử của nguyên tử Hydro - Lê Công Hảo trang 3

Bài giảng Vật lý đại cương - Chương 5: Lý thuyết lượng tử của nguyên tử Hydro - Lê Công Hảo trang 4

Bài giảng Vật lý đại cương - Chương 5: Lý thuyết lượng tử của nguyên tử Hydro - Lê Công Hảo trang 5

Tải về để xem đầy đủ hơn
File đính kèm:
 bai_giang_vat_ly_dai_cuong_chuong_5_ly_thuyet_luong_tu_cua_n.pdf
bai_giang_vat_ly_dai_cuong_chuong_5_ly_thuyet_luong_tu_cua_n.pdf



